Du jus de pommes au petit déjeuner (pour votre voiture)
25 juin 2007, posté par Yves
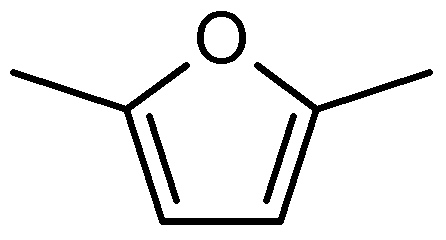
Des chercheurs étasuniens de l’université de Wisconsin-Madison ont mis au point un nouveau type de biocarburant, qui présenterait des avantages non-négligeables sur l’éthanol, à la mode ces temps-ci. Ce nouveau produit s’appelle diméthylfuran (abrégé en DMF) et le bonhomme qui fait coucou ci-dessus c’est sa structure moléculaire.
Bon mais alors les avantages sur l’éthanol? Déjà, il a 40% plus d’énergie pour un même volume (ce qui le rend comparable à l’essence habituelle), ensuite il ne s’évapore pas aussi facilement, et enfin il ne se mélange pas à l’eau, ce qui favorise entre autres son stockage. Autre point positif, ce carburant est fabriqué à base de fructose, qui est facilement extrait directement de fruits ou de plantes, ou fabriqué à partir de glucose (qu’on obtient avec de l’amidon par exemple), bref du « tout naturel » facile à produire. Mais les conséquences environnementales de son utilisation en carburant doivent encore être étudiées avant de pouvoir choisir entre « avec » ou « sans pulpe » à la pompe…
Lire d'autres articles
S'abonner au flux RSS
Partager cet article / Envoyer à un ami
A lire aussi:
alcool, automobiles, écologie, éthanol, carburant, diméthylfuran, essence, fructose, fruit.
Et pour ne pas rater les prochains billets, le mieux c'est encore de s'abonner à LiLeLa.
Postez vos commentaires dans la boîte juste en dessous.



Le 4 septembre 2007 à 12:20
LA DAME DE L’ADEME ET LES BIOCARBURANTS
Superbe exemple de parité administrative, la dame de la Dème, est en tous points conforme au modèle masculin dans les domaines techniques, comptables et fiscaux. Même inculture soixante huitarde, même langue de bois, même refus de l’évidence et des réalités physiques et financières.
Elle pérore sur les ondes autant sur le bluff de l’effet de serre que sur les biocarburants. Dans sa dernière intervention elle a expliqué que l’éthanol n’a pas les mêmes propriétés que l’alcool dit « éthylique », surtout quand, mélangé à l’essence, il devient du bi ou du diéthanol.
Selon cette dame, non seulement on sauverait l’agriculture betteravière, mais on réduirait les émissions de gaz carbonique et on ferait des tas d’économies.
Pour bien répondre il faudrait aligner des chiffres et ça, c’est fatigant à lire. On peut essayer de les remplacer par des mots.
Des labours à la pompe
Avant de sortir « l’éthanol » de l’alambic, il y a eu du travail et des dépenses d’énergie considérables.
Le tracteur qui laboure, sème et engraisse pour finir par arracher puis transporter aux camions qui continuent vers la « sucrerie » reconvertie en distillerie. Cela représente une bonne quantité de carburants. Si l’on y ajoute tout ce que consomme l’usine AZF pour produire les ammonitrates qui engraissent les terres à betteraves on obtient beaucoup de calories.
On n’a pas fini. L’usine va laver triturer malaxer, chauffer et pressurer pour sortir le jus fermentescible chargé de saccharose (le sucre). Même, si les levures travaillent sans salaires ni syndicats, elles vont consommer 33% du carbone pour produire le gaz carbonique qui fait pétiller le champagne, et les yeux de nos dames.
Ces levures vont produire de l’alcool, jusqu’au plafond de leur empoisonnement qui se situe à environ 15%, dans les mélasses, diluées en conséquence. Comme quoi les levures sont moins fragiles que les hommes qui n’en supportent que moins d’un demi pour cent de leur masse, avant le coma létal.
Ce n’est pas encore fini, car, le mélange eau alcool, limité à 12° pour des questions de productivité, devra être distillé de manière à éliminer 84% d’eau par évaporation. L’énergie nécessaire se calcule très facilement, mais il est encore plus précis d’utiliser les chiffres globaux de la comptabilité analytique de la production. En tout, il aura fallut plus d’un litre d’équivalent pétrole pour produire un litre d’alcool et il faudra 1,56 litres d’alcool pour donner l’énergie d’un litre d’essence.
Bien entendu, en brûlant ce coûteux produit, on va encore produire du gaz carbonique, ce qui devrait faire de la peine aux illusionnistes des gaz à effet de serre.
Si on raisonne, sans tenir compte de la fiscalité, comme le fit notre Ministre frisé de l’économie et des finances, mal « instruit » par son service des douanes, on peut produire l’illusion, si c’est le but cherché.
Si on est une Directrice de l’ADEME gouvernementale compétente, on doit enquêter auprès des distillateurs, analyser les comptabilités et conclure sur la comparaison de choses comparables.
Lors de sa conférence radiodiffusée sur ce sujet, le Capitaine au long cours HADDOCK (de la section Flandres-Artois en Belgique) qualifiait l’alcool d’ « ennemi du marin ». Il aurait pu ajouter « ennemi du contribuable »
Que reste-t-il de ces élucubrations avec si peu de chiffres ? Seulement la conclusion du vieux paysan :
« Si c’est pas malheureux de brûler de la nourriture »
Va-t-on encore nous parler de FAIM DANS LE MONDE ?
Pour ceux qui aiment les calculs
On retiendra les masses atomiques suivantes qui servent de base de tous les calculs : C=12 – O=16 – H=1
On notera ainsi que le sucre C12H22O11 voit sa « mole » peser : 342 grammes qui, en s’hydrolysant, vont donner 2(C6H12O6) de glucose d’une masse de 360 grammes.
A son tour la mole de glucose va fermenter en libérant 2 moles d’alcool éthylique (C2H5OH) et deux moles de gaz carbonique CO2.
En résumé on calcule facilement que 46 grammes d’alcool, avant d’être brûlés dans les moteurs, ont déjà produit 44 grammes de CO2
En brûlant, ces mêmes 46 Gr d’alcool vont encore produire 88 Gr de CO2
Soit au total 3X44 = 132 Gr de CO2 taux d’émission de CO2 132/46 = 2,87 Gr par Gramme d’alcool
L’essence, qu’on peut comparer au benzène par défaut et par précaution, a pour formule C6H6 donc une masse molaire de 78 grammes qui vont produire 264 grammes de CO2 donc taux d’émission de CO2 :
264/78 = 3,38 grammes par gramme d’essence
Or il faut 1,56 grammes d’alcool pour produire l’énergie d’un seul gramme d’essence ce qui remonte le, taux de CO2 de l’alcool à 2,87 X 1,56 = 4,48.
Vous voulez plus simple ?
1)- pour équilibrer les masses entre l’alcool et le benzène on appliquera à l’alcool le cœfficient :
78/46 = 1,696
2)- pour équilibrer les pouvoirs calorifique on multipliera ce chiffre par 1,56 soit :
1, 696 X 1,56 = 2,646
Aux 6 CO2 produits par la combustion du benzène on opposera les 3 X 2,646 = 7,94 CO2 de l’alcool.
Conclusion : 7,94/6= 1,32 à l’avantage du benzène.
L’ALCOOL GENERE AU MOINS 1,32 FOIS PLUS DE CO2 QUE NOS CARBURANTS
Si l’on ajoute à cela tout le CO2 produit en amont pour fabriquer le sucre, nul doute que les déchets de CO2 émis avec l’alcool dépassent plus que largement ce qu’on obtient avec les produits pétroliers.
Rendez vous sur internet et regardez les élucubrations verbeuses et abondantes de l’ADEME sur le sujet. On dirait la constitution giscardo-européenne adaptée aux disciplines scientifiques.
Par un écran de fumée dialectique on assiste à une démonstration visant essentiellement à faire croire à la bonne affaire.
Comment de superbes hauts fonctionnaires, issus des prestigieuses écoles de la république, comme Sciences Po ou l’ENA, peuvent-ils prendre ainsi les braves Français pour des imbéciles ?
Propager des idioties comme les gaz à effet de serre ; la pompe à chaleur (ça c’est polytechnique (voir SIROTA et l’Inspection des finances) n’est pas digne d’un pays qui, par le passé, fut à l’avant-garde des sciences.
C’est ainsi qu’on voit le triomphe d’AIRBUS (avions fabriqués à l’envers des saucissons) finir dans une panade financière incroyable et la liste est longue des fantastiques gaspillages qu’on doit à la malhonnête inculture de nos dirigeants.